Jellemzői kén
Oxigéncsoport - csoport elemek kifejezés egy kén. Vegyjeleikkel - S - az első betű a latin nevét Kén. Készítmény egyszerű anyag által rögzített szimbólum index nélkül. Tekintsük a főbb pontok tekintetében a szerkezet, tulajdonságok előállítása és alkalmazása az elem. kén funkciók kerülnek bemutatásra részletesen csak lehet.
Általános jellemzők és különbségek kalkogén
Kén vonatkozik egy alcsoportja oxigén. Ez a 16. csapat a modern hosszú ideig képet alkotnak a periódusos rendszer (PS). Elavult szobák és index - VIA. A nevét a kémiai elemek a csoport, a kémiai szimbólumok:
A külső elektron héj elemek fölött elrendezett azonos. Ez tartalmazza mind a hat vegyérték elektronok, amelyek részt vehetnek a képződését kémiai kötést létesíteni más atomokkai. Hidrogén vegyületek a következő, H2 R, például H2S - hidrogén-szulfid. Nevei kémiai elemek kialakítására oxigénnel kétféle vegyületek: kén, szelén és tellúr. Általános képletekben oxidok ezen elemek - RO2. RO3.
Kalkogén megfelelnek az egyszerű anyagok, amelyek nagyban különböznek a fizikai svostvam. A leggyakoribb a kéreg minden kalkogén - oxigén és kén. Az első elem meghatározza a két gáz, a második - a szilárd anyagok. A polónium - a radioaktív elem - ritka a földkéregben. Abban a csoportban, az oxigén polonium fémes tulajdonságok csökkentik, és növeli a fém. Például, a kén - tipikus nemfémes és a tellúr egy fémes fényezés és elektromos vezetőképesség.

№ 16 elem a periódusos rendszer DI Mengyelejev
A relatív atomsúly kén - 32,064. A leggyakoribb természetes izotóp 32 S (több, mint 95 tömeg%). Talált kisebb mennyiségben nuklidokat atomtömegű a 33., 34. és 36. jellemző kén a helyzet az SS, és atomi szerkezetének:
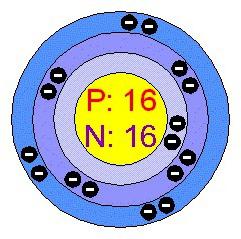
- sorozatszáma - 16;
- felelős a atom 16;
- atomrádiusz - 0,104 nm;
- ionizációs energiája -10,36 eV;
- relatív elektronegativitási - 2,6;
- az oxidáció mértékét a vegyületek - +6, +4, +2, -2;
- vegyértéke - II (-), II (+), IV (+), VI (+).
A kén a harmadik periódusban; elektronok egy atom található három energia szintje: az első - 2, a második - 8, - a harmadik 6. vegyérték elektronok mind a külső. Amikor kölcsönhatásban elemekkel elektronegatívabb kén ad 4 vagy 6 elektronok, megszerzése tipikus oxidációs állapotban +6, +4. A reakciókat hidrogénnel és egy fématom vonzza az elektronokat, a hiányzó két oktett, hogy töltse és elérni egyensúlyi állapotban. Az oxidációs ebben az esetben csökkentjük -2.
A fizikai tulajdonságok a rombusz és a monoklin allotropic formák
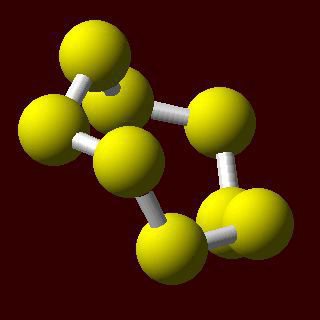
Normális körülmények között, a kén atomok egymáshoz szögben stabil áramkörben. Ők lehet zárva egy gyűrű, ami arra utal, a létezését gyűrűs kéntartalmú molekulák. Összetétele tükrözi S6 és S8 formula.
kén jellemzői kell egészíteni leírás közötti különbségeket allotropic módosítások, amelyek a különböző fizikai tulajdonságokkal.
Rombusz vagy α-kén - a legstabilabb kristályos formában. Ez a világos sárga kristályok álló S8 molekulák. rombusz kén sűrűsége 2,07 g / cm3. A világossárga kristályok monoklin formájának β-kialakult kén sűrűséggel 1,96 g / cm3. Forráspont eléri 444,5 ° C-on
Amorf kén
Milyen színű kén képlékeny állapotban? Ez egy sötétbarna massza, nagyon hasonló a sárga por vagy kristályok. Ahhoz, hogy ez, meg kell, hogy olvad a rombusz vagy monoklin kén. Feletti hőmérsékleten 110 ° C-on egy folyadék képződik, míg a további melegítés elsötétedik 200 ° C-on válik sűrű és viszkózus. Ha gyorsan öntsük olvadt kén hideg vízbe, megkeményedik alkotnak cikkcakkos láncok, amelyek szerkezete tükrözi a képlet Sn.

A oldhatósága kén
Bizonyos módosítások az oldódó anyagot szén-diszulfidban, benzolban, toluolban, vagy cseppfolyós ammóniával. Ha lassan lehűtjük szerves oldatokat ezután kialakítva monoklin kén tűk. Elpárologtatására folyadékok állni egyértelmű citrom-sárga kristályok a rombusz kén. Ők törékenyek, könnyen őrölni a por. A kén nem oldódik vízben. A kristályokat aljára süllyednek a hajó, és a por a felületen lebegtek (nem nedvesíthető).
kémiai tulajdonságok
A reakciókat mutatjuk tipikus nemfémes elemet tulajdonságok № 16:
- kén oxidálódik fémek és a hidrogén, csökken S 2- ion;
- az égési levegő és az oxigén előállított di- és kén-trioxid, amelyek savanhidridek;
- reagáltatva egy másik nagyobb elektronegativitású elem - fluor - Kén is elveszti elektronok (oxidálódnak).
A szabad kén a természetben
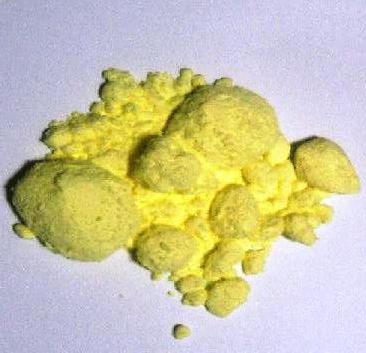
Milyen színű kén jellegű (natív)? Ez a halványsárga por, jellegzetes szagú vagy sárga kristályos anyagként, amely üvegből csillogás. Betétek betétek formájában, kristályos rétegek kén területén találhatóak az ősi és modern vulkáni Olaszországban, Lengyelországban, a Közel-Keleten, Japánban, Mexikóban, Egyesült Államok. Gyakran a kitermelés drusenek egy gyönyörű és hatalmas egykristály.
Hidrogén-szulfid és oxidok a természetben
A vulkanikus régiókban találhatók a felszínen a gáz-halmazállapotú kén vegyületet. Fekete tengeri mélységben több mint 200 m-élettelen, mert a hidrogén-szulfid H2 S. A képletű kétértékű kénatomhoz oxid - SO2. Trivalens - SO3. Ezek a gáz alakú vegyületek vannak jelen a készítményben néhány olaj, gáz, természetes vizek. Kén benne van a készítmény szén. Szükséges, hogy az építési számos szerves vegyület. Amikor elrohadásának fehérjék csirke tojás felszabaduló hidrogén-szulfid, így gyakran azt mondta, hogy a gáz szaga rothadó tojás. Kén tartozik a biogén elemek, szükség van a növekedés és fejlődés a férfi, állatok és növények.

Jelentősége természetes szulfidok és szulfátok
Jellemzői kén lesz teljes, ha nem azt, hogy az elem megtalálható nem csak a formája egy egyszerű anyag és az oxid. A leggyakoribb természetes vegyületek - egy só kénsav és hidrogén-szulfidot. Szulfidok réz, vas, cink, higany, ólom megtalálható az összetétele a ásványok kalkopirit, pirit, szfalerit, galenit, és cinóber. Szulfátoktól említhetjük a nátrium, kalcium, bárium és magnézium-sók, amelyek alkotják a természetben ásványok és kőzetek (mirabilit, gipsz, szelenit, barit, kieserit, epsomite). Mindezen vegyületeket használnak a különböző ágazatokban a gazdaság, a nyersanyagként használt ipari feldolgozásra, műtrágyák, építőanyagok. Nagy gyógyászati értékét az egyes kristályos.
sárga anyag szabad állapotban fordul elő a természetben különböző mélységben. Ha szükséges, a kén megolvad kőzetekből emelése nélkül őket a felszínre, miközben szivattyúzás mélysége túlhevített gőzzel és sűrített levegővel. Egy másik módszer a szublimációs kőzúzalék speciális kemencék. Más eljárások során oldódási szén-diszulfidot vagy flotációs.
Ipari követelmények kén nagy, így kapunk elemi használt anyag vegyületet. A hidrogén-szulfid és a szulfid-ként van redukált formában. A oxidációs állapota az elem megegyezik -2. Kén végrehajtott oxidáció növelésével a 0 érték Például, a módszer a LeBlanc nátrium-szulfát csökken -szulfid szén. Ezután kapjuk a kalcium-szulfid, ez szén-dioxiddal kezeljük, és a vízgőz. A kapott hidrogén-szulfidot oxidáljuk, légköri oxigénnel katalizátor jelenlétében: 2H2 S + O2 = 2H2 O + 2S. A kéntartalom meghatározása sokféle módon, néha ad alacsony tisztaságú mutatók. Finomítás vagy a tisztítást végzett desztillációval, helyesbítését, feldolgozási savak keverékei.

A kén alkalmazása a modern ipar
Kén granulátum megy különböző termelési igények:
- Előállítása kénsav a vegyiparban.
- Termelés szulfitok és szulfátok.
- Leadású készítmények Trágyazás növények, a betegség és a kártevők.
- Kéntartalmú érc bányászati és vegyi üzemekben feldolgozott fémekhez. Egyidejű termelés kénsav.
- A bevezetése bizonyos minőségű acélból kölcsönöz különleges tulajdonságait.
- Due vulkanizáljuk gumi kapunk gumi.
- Termelés mérkőzést, pirotechnika, robbanóanyag.
- Használja előállítására festékek, pigmentek, szintetikus szálak.
- Fehérítése szövet.

Toxicitás A kén és vegyületei
A porokat részecskék kellemetlen szag, irritálják a nyálkahártyákat az orrüreg és a légutak, a szem és a bőr. De az elemi kén mérgező hatása nem tekinthető különösen magas. Belélegzés a hidrogén-szulfid és széndioxid okozhat súlyos mérgezést.
Ha pörkölés kéntartalmú érc kohók kipufogógázok ne szoruljanak, belépnek a légkörbe. Csatlakozó a csepp és a vízgőz, kén-oxidok, nitrogén-vezetnek az úgynevezett savas eső.
A kén és vegyületei a mezőgazdaságban
Növények fogyasztanak szulfátionok együtt talajoldattal. Kéntartalmának a csökkentése vezet lassítják a zöld sejtek anyagcseréjét aminosavak és fehérjék. Ezért szulfátok használt mezőgazdasági termények trágyázására.

Fertőtleníthető baromfi házak, pincék, növényi üzletek egyszerű anyag égett vagy kezeljük modern létesítmények szulfonamidok gyógyszerek. kén-oxid antimikrobiális tulajdonságokkal, hogy már régóta megtalálható alkalmazás a bor előállítására, amikor tárolt zöldségek és gyümölcsök. kén gyógyszereket használnak, mint peszticidek kontrollálására betegségek és kártevők (lisztharmat és takácsatkák).
Használják a gyógyászatban

Nagy jelentőséget tulajdonítanak a tanulmány gyógyszer tulajdonságait sárga por adta nagyszerű orvosok ókor Avicenna és Paracelsus. Később megállapították, hogy nem kap elég kén élelmiszer gyengül, egészségügyi problémák (amely magában foglalja a viszketés és hámlás a bőr, a haj és a körmök gyengülése). A tény az, hogy anélkül, hogy a kén felület szintézisét aminosavak, keratin, biokémiai folyamatokat a szervezetben.
Orvosi kén beépül a kenőcsöt a bőrbetegségek kezelésére: akne, ekcéma, pikkelysömör, allergia, seborrhea. Fürdők kénnel enyhíti a fájdalmat a reuma és a köszvény. A jobb felszívódását a szervezetben, hogy hozzon létre vízoldható szulfonamid gyógyszerek. Ez nem egy sárga por, finom kristályos fehér anyagot. Kültéri alkalmazások ezt a vegyületet adjuk a kozmetikai bőrápoló.
Gipsz már régóta használják a rögzítését a sérült testrész. Glnubersó írja elő, mint hashajtó gyógyszert. Magnesia csökkenti a vérnyomást, hogy használják a magas vérnyomás kezelésére.
Kén történelem
Már az ókorban nem fémes anyag sárga virágok vonzzák a személy figyelmét. De csak 1789-ben, a nagy vegyész Lavoisier találtuk, hogy a por és a kristályok a természetben található, tagjai kénatomot. Azt hitték, hogy a kellemetlen szag során felmerülő, az égés, taszítja minden gonosz. Formula kén-oxidot, amelyet úgy kapunk, égés, - SO 2 (-dioxid). Ez mérgező gázok belélegzése ez veszélyes az egészségre. Több esetben tömeges kihalás egész falvak emberek a partok, az alföldön a tudósok magyarázzák a földhasználati vagy a víz hidrogén-szulfid vagy kén-dioxid.
A találmány a puskapor fokozott érdeklődést színű kristályok alakjában a katonai. Sok csatát nyertek köszönhető, hogy a mesterek, hogy összekapcsolják a kén más anyagokkal a robbanóanyagok gyártásához. A legfontosabb vegyülete - kénsav - is megtanulta, hogyan kell használni egy nagyon hosszú idő. A középkorban, hogy egy anyag, a olaj vitriol és só --szulfát. Réz-szulfát CuSO4 és vas-szulfát FeSO4 még nem veszítették el jelentőségét az iparban és a mezőgazdaságban.

