Molekuláris fizika és termodinamika
Grafikusan, adiabatikus eljárást ismertetnek a (p, V) - görbék hasonló diagramot izoterma (2.12 ábra.), Azonban a növekedés eléri meredekebb, hiszen g> 1. a Cp> CV.
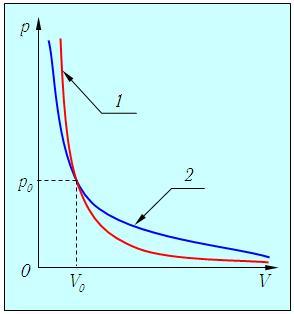
Ábra. 2.12. Adiabatikus folyamat az ideális gáz: 1 - adiabatikus, 2 - izoterma
Ez érthető, hiszen a gáz adiabatikus tágulása végez működik, mert a belső energia, és annak hőmérséklet csökken, ami tovább csökkenti a nyomást képest izotermikus expanzió.
Kísérleti vizsgálata adiabatikus folyamatok ideális gáz alkalmazásával lehet végezni a ábrán bemutatott berendezést. 2.13.
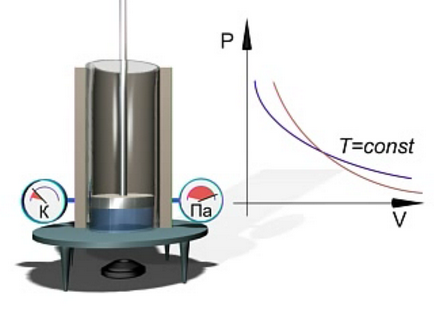
Ábra. 2.13. Kísérleti vizsgálata adiabatikus folyamatok ideális gáz
Tekintettel arra, hogy a ideális gáztörvény arányosnak kell lennie
Az egyenlet a adiabatikus folyamat is írható
A termodinamika első főtétele alkalmazni a adiabatikus folyamat gáz biztosítja a működést számított adiabatikus:
Kifejezések egy adiabatikus folyamat, ha figyelembe vesszük Clapeyron egyenlet - Mendeleev is kifejezhető az a hőmérsékletet, az elején és végén a folyamat
Példa. Az éghető keverék a dízelmotor (lásd. A fenti ábrát) meggyullad hőmérsékleten T2 = 1100 K. A kiindulási elegy hőmérséklete T1 = 350 K. Definiáljuk, hogy hányszor kell csökkenteni a hangerőt a keverékben a kompresszió alatt, úgy, hogy lángra. Compression kell tekinteni adiabatikus. adiabatikus index a keverék g = 1,4.
Hogy oldja sokkal kényelmesebb használni az egyenlet a adiabatikus folyamat formájában (2,31):
Ebből következik, azonnal, hogy a kifejezés a kompressziós mértéke a tüzelőanyag-keverék: