Adiabatikus folyamat - studopediya
A fő paraméterek, amelyek jellemzik az állam a gáznyomás P. van a V térfogat és hőmérséklet T. közötti kapcsolat ezeket a paramétereket az ideális beállított Mengyelejev-Clapeyron egyenlet:
ahol M - tömege egy mól gáz, kg / mol; m - tömege gáz, kg; T - abszolút gáz hőmérséklete, K; R = 8,31 J / (mol × K), - az univerzális (moláris) gázállandó.
Ha van két három alapvető paramétereit, a gáz, a harmadik lehet kifejezni rajtuk keresztül. Ha megváltoztatja a három paraméter a gáz kezdeti paraméterek (P1. V1. T1) társított az új paraméterekkel az azonos mennyiségű gáz (P2. V2. T2) egyenletet.
Adiabatikus folyamatorientált olyan folyamat, amely nélkül zajlik hőcsere a környezettel. azaz Q = 0.
Adiabatikus folyamatot végezhetjük a rendszerben, körülvéve egy hőszigetelő (adiabatikus) héj. Egy példa erre a folyamatra - a munkaciklus a hőerőgép, ahol a gáz (gőz) a hengerben kitágul hőszigetelő falakkal és a dugattyú, a hiányában irreverzibilis transzformációk súrlódási munka hővé. Adiabatikus folyamatot végre lehet hajtani hiányában adiabatikus héj; erre kell folytatni olyan gyorsan, hogy a folyamat során a hőátadás történt a rendszer és a környezet.
Az első főtétele jelentése:
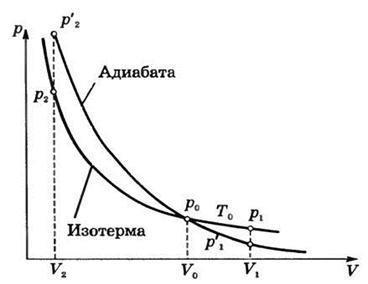
Ez azt jelenti, hogy ha egy adiabatikus folyamat, a rendszer végezhet munkát külső szervek csak a veszteséget belső energia. Ha A> 0, # 916; U = -A <0, т.е. U2 Mint ismeretes, a gáz végez munkát, ha # 916; V> 0. Így, ha adiabatikus gáz végez munkát maga lehűtjük. Ezzel szemben, ha egy adiabatikus kompresszió (A <0 ) над газом совершается работа и газ нагревается . Amikor adiabatikus folyamat nyomás és térfogat kapcsolódnak az alábbi egyenlettel: p × V g = const vagy p × T g / (g - 1) = const, ahol # 947> 1 - arányban specifikus futamok (vagy Poisson-tényező). Ez az egyenlet az úgynevezett adiabatikus egyenlet vagy a Poisson-egyenlet. S entrópia változás a rendszer reverzibilis adiabatikus folyamat miatt a hőátadás a határ a rendszer nem kerül sor: Amennyiben T - a hőmérséklet a rendszer, # 948; Q - hő rendszer által kapott. Ennek köszönhetően a adiabatikus folyamat része lehet egy reverzibilis ciklus. Adiabatikus állapotváltozás a gáz fejezhető grafikusan. A grafikon az ezt a folyamatot nevezik adiabatikus (ábra. 2). Amikor ugyanazt a kezdeti feltételeket (p0. V0) gyorsabban csökken a adiabatikus tágulása a gáz nyomása, mint izoterm, mert okozott nyomásesés nemcsak a mennyiségi növekedés (egy izotermikus expanzió), hanem egy hőmérséklet-csökkenés. Ezért alá megy adiabatikus és izotermikus gáz adiabatikus nem kevesebb munkát, mint az izotermikus expanzió.
A gyors tömörítés (bővítés) a hő nem volt ideje, hogy fordulhat elő, és a folyamatok is tekinthető adiabatikus (egyensúlyi). Ezért, bármilyen gáz fűtése gyors összenyomó (például, hőszivattyú felfújásakor kerékpár gumiabroncsok). Ha egy erős és gyors kompressziós hőmérséklet emelkedhet úgy, hogy jelenlétében a benzin gőzök a levegőben vannak lángra. Ezt használják a dízelmotorok meggyújtására éghető keverék. Ez magyarázza, hogy szükség van egy külön hűtési teljesítményű kompresszorok.
Hűtés alatti levegő adiabatikus képződését okozza felhők.